技術資料
ー珪酸塩の性質ー
技術資料 ー 珪酸塩の性質
珪酸塩無水物について
i ) 融点
アルカリ金属酸化物(M2O)とSiO2の二成分系の融点の相平衡図は次のようになっています。
 |
| (Ⅰ)2LiO2・SiO2 Field |
| (Ⅱ)Li2O・SiO2 Field |
| (Ⅲ)LiO2・2SiO2 Field |
| (Ⅵ)Na2O・SiO2 Field |
 |
| (Ⅶ)Na2O・2SiO2 Field |
| (Ⅷ)K2O・SiO2 Field |
| (Ⅸ)K2O・2SiO2 Field |
| (Ⅹ)K2O・4SiO2 Field |
 |
| (ⅩⅩⅠ)Quarz Field |
| (ⅩⅩ)Tridimite Field |
| (ⅩⅨ)Cristobalite Field |
この図からオルソ珪酸塩、メタ珪酸塩、二珪酸塩、珪酸カリウム系では他にテトラ珪酸塩の結晶の存在を示しています。これらの結晶はナトリウム塩の場合モル比1.2以下の低モル比 の状態で急速に結晶化が進むのであってそれ以上のモル比ではその結晶化は非常に緩慢でありそのため現実に製造しているガラスは上記の表の様な明確な融点を示しません 。
i i ) 珪酸ソーダ、珪酸カリのガラスの軟化点、及び流動点
| モル比 SiO₂/M₂O | SiO2 % | M2O % | 軟化点 ℃ | 流動点 ℃ |
| 珪酸ソーダ | ||||
| 3.87 | 79.0 | 21.0 | 665 | 870 |
| 3.33 | 76.3 | 23.7 | 655 | 840 |
| 3.00 | 74.4 | 25.6 | 640 | 825 |
| 2.48 | 70.6 | 29.4 | 615 | 790 |
| 2.07 | 66.7 | 33.3 | 590 | 760 |
| 1.65 | 61.5 | 38.5 | 565 | 730 |
| 1.00 | 49.2 | 50.8 | … | 1089 |
| 珪酸カリ | ||||
| 3.92 | 71.4 | 28.6 | 690-740 | 910 |
| 3.30 | 67.7 | 32.3 | 690-740 | 890 |
軟化点 - 粘度 4 × 107 P
流動点 - 粘度 105 P
珪酸塩水溶液について
i)珪酸イオンについて
珪酸塩水溶液での珪酸イオンは六配位であってモノマー、ダイマー、トリマーそれ以上のポリマー、それにコロイダルなイオンミセルがあり、夫々の割合は、濃度、モル比(SIO2/M2O)、陽イオンの種類により変化します。
メタ珪酸塩、或いはそれより低モル比の水溶液ではモノマーが大部分を占めています。ポリマーイオン濃度はモル比の上昇により増加します。光散乱法によって測定された珪酸イオンの重量一平均分子量は次の様に報告されています。
| 各モル比に於いての珪酸ソーダ、珪酸カリの重量平均分子量 | |||
| 珪酸ソーダ(SiO2/Na2O) | 珪酸カリ(SiO2/K2O) | ||
| モル比(SiO2/Na2O) | wt av moi wt in Soin | モル比(SiO2/K2O) | wt av moi wt in Soin |
| 0.48 | 60 | 1.00 | 56 |
| 1.01 | 90 | 1.75 | 115 |
| 1.69 | 120 | 2.50 | 295 |
| 2.09 | 160 | 2.80 | 304 |
| 2.62 | 265 | 3.31 | 495 |
| 3.30 | 320 | 3.62 | 620 |
| – | – | 3.97 | 848 |
オルソ、メタ珪酸ソーダは水中で次の様に解離していると思われます。
オルソ珪酸ソーダの場合
①Na4SiO4 + H2O → Si(OH)6= + 4Na+ + 2OH–
メタ珪酸ソーダの場合
①Na2SiO3 + Si(OH)6 + 2Na
②Si(OH)6 ⇔ Si(OH)4 + 2OH
③2Si(OH)4 ⇔ (H.O)3-Si-O-Si(OH)3 + H2O
(二重体)
となり少量の二重体も存在すると思われます。
次いで陽イオンの影響としては次のような現象があります。
Na+の場合
モル比が4.0以上、SIO2濃度が10%以上では、不安定でゲル化し易い
K+の場合
モル比4以上でSiO2濃度が10%以上では粘性が急激に上昇
Li+の場合
モル比8、SiO2 20%でも室温では安定(高温では不安定)であり粘性も低い
以上の様な現象は水和された陽イオン半径によるものと思われる。
各陽イオンの性質は次の表にしめす。
| 水溶液中で配意数6のアルカリ金属のイオンの比較 | ||||||
| Li | Na | K | Rb | Cs | ||
| イオン半径A° | 0.60 | 0.95 | 1.33 | 1.48 | 1.69 | |
| 水和イオン半径A° | 3.40 | 2.76 | 2.32 | 2.28 | 2.28 | |
| hydration number | 25.3 | 16.6 | 10.5 | 9.9 | ||
| hydration energy Kcal/mol | 12.3 | 9.7 | 7.7 | 7.0 | 6.3 | |
ii) 水素イオン濃度(pH)
夫々の珪酸塩のpH価は次の図の様になります。
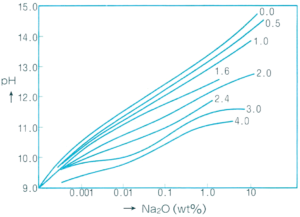
珪酸ナトリウム
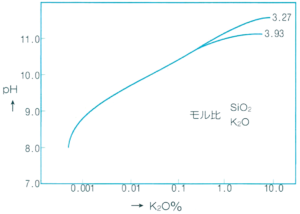
珪酸カリウム
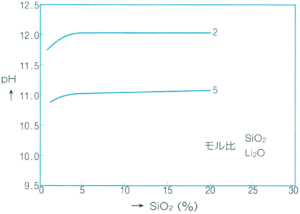
珪酸リチウム
珪酸塩溶液のpHはモル比が高い程pH価は低下しますが、その緩衝能力は増加します。
iii) 粘度
各種珪酸塩の濃度は下記の図に示します。
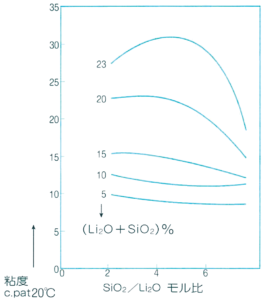
珪酸リチウム
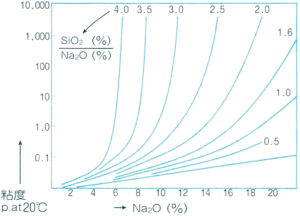
珪酸ナトリウム
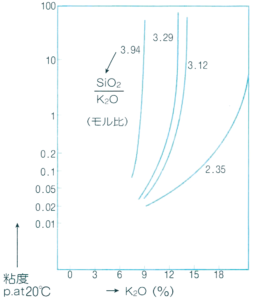
珪酸カリウム
iv ) 珪酸ソーダの比重と成分の関係
次の図-4 は20℃に於ける比重(Be’)と重量比(SiO2(%)/Na2O(%))との 関係を示しています。これらBe’、Na2Oの量(%)、SiO2の量(%)の三成分 のうち二つの成 分の量を知る事により残りの成分の概略値を得ようとする場合、便利なグラフとして利用されています。
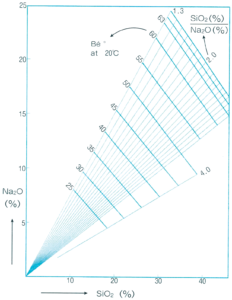
20℃に於けるBe’は次式により得る事が出来ます
Be’20℃=Be’t°+ 0.04(t°- 20°)
Be’より比重を求める時は次式により得られます。
d = 144.3 ÷ (144.3 – Be’)
Be’ = 144.3 – (144.3 / d)
v) 各珪酸塩の濃度、比重、粘度、pHの値を下表にとりまとめました。
| Na-Silicate | ||||||
| 重量比 (SiO2/Na2O) | モル比 SiO2/Na2O | Na2O | SiO2 | d20(比重) | ViS (20℃c.p) | pH |
| 1.6 | 1.65 | 19.5 | 31.2 | 1.68 | 7,000 | 12.8 |
| 2.0 | 2.07 | 18.0 | 36.0 | 1.69 | 70,000 | 12.2 |
| 2.5 | 2.58 | 10.5 | 26.3 | 1.41 | 50 | 11.7 |
| 2.9 | 3.00 | 11.0 | 31.9 | 1.49 | 960 | 11.5 |
| 3.22 | 3.33 | 8.9 | 28.7 | 1.39 | 180 | 11.3 |
| 3.75 | 3.88 | 6.8 | 25.5 | 1.32 | 220 | 10.8 |
| K-Silicate | ||||||
| 重量比 (SiO2/K2O) | モル比 SiO2/K2O | K2O | SiO2 | d20(比重) | ViS (20℃c.p) | pH |
| 2.50 | 3.92 | 8.3 | 20.8 | 1.26 | 40 | 11.30 |
| 2.20 | 3.45 | 9.05 | 19.9 | 1.26 | 7 | 11.55 |
| 2.5 | 2.30 | 12.5 | 26.3 | 1.38 | 1,050 | 11.70 |
| 2.10 | 2.83 | 16.4 | 29.5 | 1.49 | 1,300 | 12.15 |
| Li-Silicate | |||||||
| 重量比 (SiO2/Li2O) | モル比 SiO2/Li2O | Li2O | Na2O | SiO2 | d20(比重) | ViS (20℃c.p) | pH |
| 9.4 | 4.7 | 2.2 | - | 20.7 | 1.17 | - | - |
| 9.6 | 4.8 | 2.1 | - | 20.0 | - | 40 | 11.0 |
| 11.8 | 5.9 | 1.6 | - | 18.8 | 1.18 | - | - |
| 17.0 | 8.5 | 1.2 | - | 20.0 | - | 25 | 11.0 |
| SiO2/Li2O+Na2O | SiO2/Li2O+Na2O | ||||||
| 6.5 | 4.1 | 1.8 | 1.2 | 19.6 | 1.19 | - | |



